Ione ammonio, utilizzato durante alcuni processi per la tinteggiatura della lana, è uno ione che ha qualcosa a che fare con l’ammoniaca, come il nome ci suggerisce, ma che troviamo anche in concentrazioni non abbastanza basse nel particolato atmosferico. Purtroppo perché non è tra le sostanze che è bene respirare come nemmeno lo sono i COV e i NOx.
Ione ammonio in acqua
Lo ione ammonio si forma in soluzione acquosa di ammoniaca e il suo comportamento può essere affiancato a quello di un metallo alcalino. Esiste anche l’acetato di ammonio, anzi, ne esistono due di cui uno neutro e uno acido, rispettivamente CH3COONH4 e CH3COONH4∙CH3COOH.
Questo ione è uno dei pochi poliatomici, per formarlo si aggiunge all’ammoniaca uno ione H+ in modo che tra essi si formi un legame di coordinazione, ovvero un legame chimico covalente in cui una coppia di elettroni viene messa a disposizione direttamente da un solo atomo, mentre l’altro atomo che contrae il legame non utilizza elettroni propri in compartecipazione bensì sfrutta la coppia “donata” dal primo atomo.
Queste erano le premesse, forse un po’ tecniche, ma necessarie, per andare a descrivere il comportamento dello ione ammonio in acqua. Esso di solito viene messo in acqua come componente di un sale e si verifica il fenomeno dell’idrolisi, il risultato è quello di un ambiente acido.

Ione ammonio acido
Questo ione spesso viene usato come acido debole perché può protonare una base più forte utilizzando uno dei quattro atomi di idrogeno e tornando così ad essere ammoniaca. Possiamo considerare lo ione ammonio l’acido coniugato della base ammoniaca, se prendiamo una soluzione, per sapere quanto e come l’ammoniaca “diventerà” ione ammonio dobbiamo guardarne il pH.
Ione ammonio: struttura
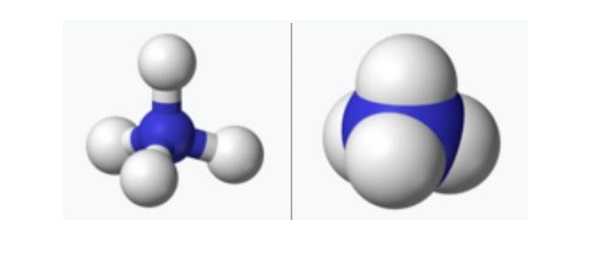
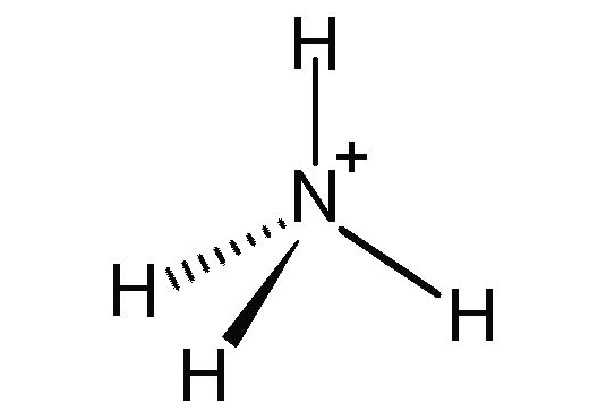
Prendiamo un atomo di azoto che di base ha una struttura con ibridazione sp3, è al centro di un tetraedro regolare con vertici occupati da atomi di idrogeno, atomi di idrogeno equivalenti. Quando l’azoto viene caricato positivamente forma 4 legami covalenti invece che i tre che ci sono nella struttura dell’ammoniaca. Si tratta di una reazione chimica, di una reazione chimica che è reversibile.
Ione ammonio e particolato atmosferico
Troviamo lo ione ammonio anche nelle analisi del particolato atmosferico durante le quali si cerca di classificare dal punto di vista fisico ciò che si trova nell’aria dividendolo innanzitutto in tre classi principali. In quella degli ioni inorganici troviamo quello di ammonio assieme a solfati e nitrati, una seconda classe è quella costituita dalla frazione carboniosa del particolato atmosferico che comprende sia il carbonio organico sia quello elementare, poi c’è la classe costituita dal così detto “materiale crostale”.
Possiamo immaginarlo associato al pulviscolo atmosferico oppure come assieme di elementi presenti solo in tracce. Queste tre grandi classi, assieme ad una componente di acqua non meglio identificata, vanno a formare il materiale particolato che ha dimensioni molto differenti, tanto che si misura sia il PM2,5 sia il PM10.

Ione ammonio: Iupac
Ione poliatomico caricato positivamente, quello ammonio ha la seguente formula chimica: NH4+. La sua massa molecolare è apri a 18,04 g/mol e il suo numero CAS 6684-80-6. La reazione che ci da il nostro ione è:
NH3 + H+ → NH4+. Questo ione, solo come alcuni altri raggruppamenti cationici, ha un nome che nasce dall’aggiunta della desinenza –ONIO. Non accade sempre così.
Se vi è piaciuto questo articolo continuate a seguirmi anche su Twitter, Facebook, Google+, Instagram
Ti potrebbe interessare anche:
